Double Outlet Right Ventricle (DORV)
Ein sogenannter Double Outlet Right Ventricle (DORV) ist ein angeborener Herzfehler, bei dem sowohl die Lungenschlagader (Pulmonalarterie, PA) als auch die Hauptschlagader (Aorta) zum überwiegenden Teil aus der rechten Herzkammer entspringen. Außerdem gibt es einen Defekt der Kammerscheidewand (Ventrikelseptumdefekt, VSD); und die großen Gefäße Aorta und PA können rechts oder links, voreinander oder nebeneinander aus der rechten Kammer entspringen. Weiterhin kann es Engstellen (Stenosen) der rechten und linken Ausstrombahn geben.
Varianten
Es gibt viele unterschiedliche DORV-Varianten, die bei Patient:innen zu ganz verschiedenen Symptomen führen. Dementsprechend muss die Behandlung differenziert und individuell erfolgen.
Vor einer Korrekturoperation funktioniert das Herz wie ein Einkammerherz. Ein wesentlicher Einflussfaktor, der die Dringlichkeit und den Zeitpunkt der operativen Behandlung bestimmt, ist der Blutfluss zu den Lungen. Ist dieser z.B. durch eine Einengung der Lungenschlagader behindert, können die Säuglinge kurz nach der Geburt an Blausucht (Zyanose) leiden und benötigen eine rasche Therapie, die den Blutfluss zur Lunge verbessert.
Ist der Blutfluss zur Lunge frei, kann eine Lungenüberflutung die Therapie auch schon in den ersten Lebensmonaten erforderlich machen. Ist der Blutfluss zur Lunge ungefähr so groß wie der zum Körper (balanciert), dann wird die Korrektur meist im vierten bis sechsten Lebensmonat durchgeführt.
Man unterscheidet verschiedene DORV-Varianten, deren Korrektur unterschiedlich kompliziert sein kann:
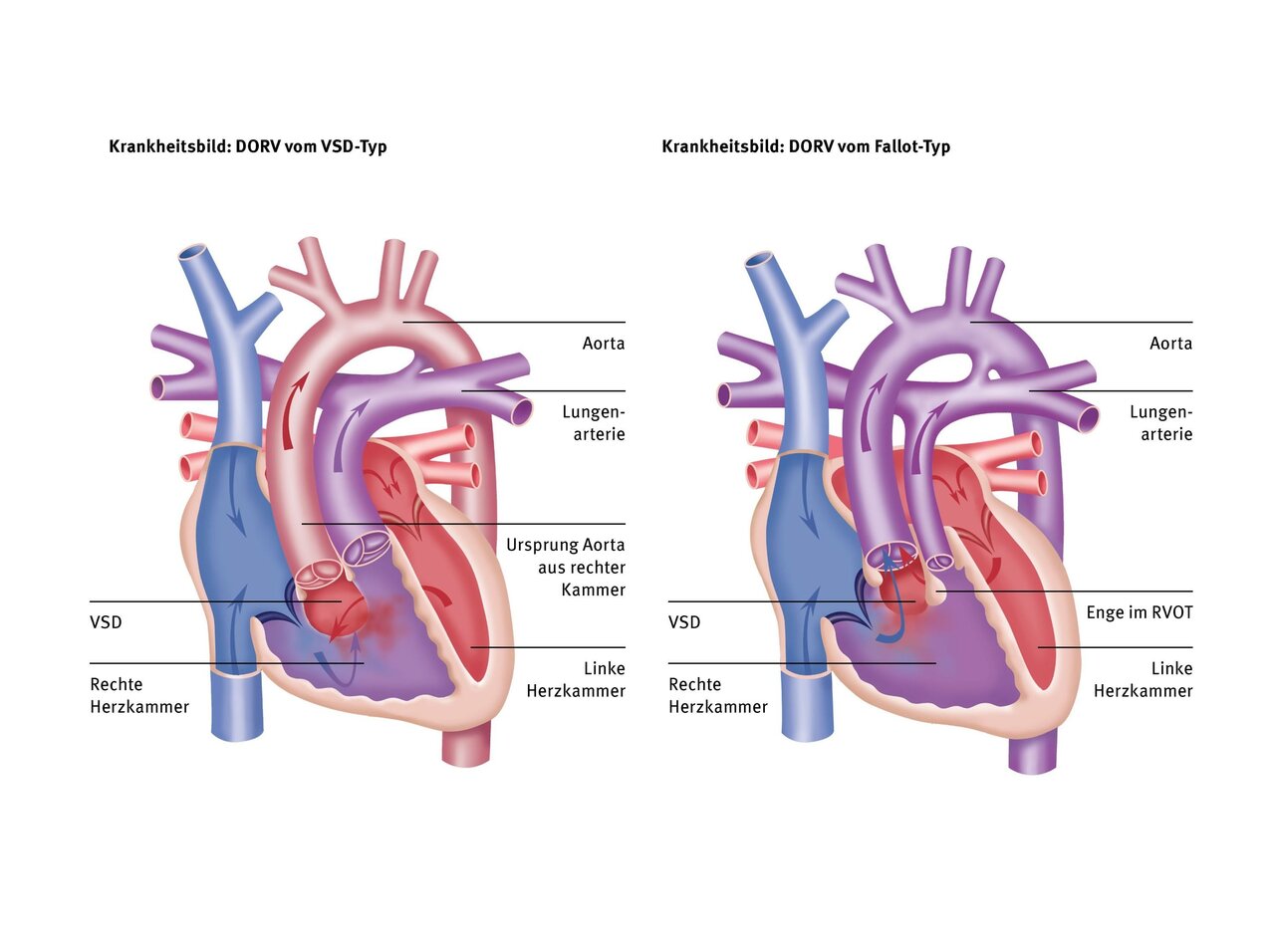
Bei diesem Typ entspringt die Lungenschlagader zu 100 % und die Aorta zu etwas mehr als 50 % aus der rechten Kammer. Der VSD liegt nahe an der Aortenklappe, wie bei einem „normalen“ VSD ohne Verengung der Lungenschlagader. Durch den Fluss des Blutes von links nach rechts über den VSD kann es daher wie auch beim VSD zur Lungenüberflutung kommen.
Bei diesem Typ stehen die Gefäße ähnlich wie beim DORV vom VSD-Typ. Allerdings gibt es hier eine Verengung des rechten Ausflusstraktes bzw. der Lungenschlagaderklappe, welche den Fluss über den VSD in die Lunge beschränkt. Bei diesem Typ kommt es also nicht zur Lungenüberflutung. Durch den geringeren Fluss in die Lunge kann es jedoch bei ausgeprägter Enge der rechten Ausstrombahn zur Sauerstoffarmut/Blausucht kommen, ähnlich wie bei einer Fallot’schen Tetralogie (TOF).
Bei diesem Typ sind die Lungenschlagader und Aorta vertauscht wie bei einer normalen Transpositionsstellung der großen Gefäße (TGA). Das führt dazu, dass die Aorta zu 100 % und die Lungenschlagader zu weniger als 50 % aus der rechten Herzkammer entspringt. Der VSD kommt dadurch unterhalb der Lungenschlagaderklappe zu liegen. Eine Enge im Bereich der rechten Ausstrombahn kann bestehen und kann zu einem geringeren Wachstum der Aorta und des Aortenbogens führen. Der Blutfluss in Richtung der Lunge ist frei, was zu einer Lungenüberflutung führen kann.
Diese Sonderform des DORVs ähnelt dem TGA-Typ, jedoch stehen die beiden großen Gefäße nicht vorne und hinten, sondern nebeneinander „Seite bei Seite“, wobei die Aorta weiter rechts und die Lungenarterie weiter links zu liegen kommt und über dem VSD reitet. Der VSD liegt anders als beim TGA-Typ weit im Auslassteil der rechten Kammer. Die Aorta entspringt zu 100 % aus der rechten Kammer und es besteht oft eine Enge unterhalb der Aortenklappe, was dazu führen kann, dass die aufsteigende Aorta und der Aortenbogen schmal (hypoplastisch) ist und bei der Korrekturoperation ebenfalls erweitert werden muss. Beim Taussig-Bing Herz kann es zur Lungenüberflutung und gleichzeitig zu einem geringen Fluss in die Aorta kommen.
Bei diesem Typ, welcher gleichzeitig auch der komplexeste Typ des DORV-Spektrums ist, kommen beide großen Gefäße zu 100 % aus der rechten Kammer, weshalb wir diesen Typ auch als „200 % DORV“ bezeichnen. Der VSD ist ein sogenannter „non-committed VSD“ was bedeutet, dass dieser keinem großen Gefäß zugeordnet ist, sondern weit entfernt davon liegt. Dies macht eine Korrektur meist schwieriger, weil der Tunnel in der rechten Kammer vom VSD zur Aorta meist lang ist und so geschaffen werden muss, dass es weder zu Engstellen im Bereich der rechten Einstrom- oder Ausstrombahn kommt.

Symptome
Abhängig von dem Typ des DORVs und abhängig von der Größe und Lagebeziehung des VSDs sowie einer eventuell bestehenden Enge der rechten Ausstrombahn, können unterschiedliche Symptome zu unterschiedlichen Zeitpunkten auftreten.
Beim DORV vom VSD-Typ kommt es durch den vermehrten Blutstrom über den VSD von links nach rechts zur Lungenüberflutung, wenn diese nicht durch eine zusätzliche Engstelle der rechten Ausstrombahn „geschützt“ wird. Dies kann sich durch Schwitzen, eine Trinkschwäche, vermehrte respiratorische Infekte und eine Gedeihstörung äußern.
Beim DORV vom Fallot-Typ hingegen kommt es ähnlich wie bei der Fallot’schen Tetralogie, in Abhängigkeit von der Ausprägung der Engstelle der rechten Ausstrombahn zu einem schlechteren Blutfluss in die Lunge. Das Blut hat also keine hundertprozentige Sauerstoffsättigung mehr, sondern ist schlechter mit Sauerstoff angereichert. Diese niedrigere Sauerstoffsättigung (z.B. nur 75%) äußert sich dann als blaue Verfärbung der Haut (Zyanose), die man am besten an den Lippen der Kinder bemerken kann.
Beim DORV vom TGA-Typ kommt es durch die beiden „vertauschten“ großen Gefäße und den unterhalb der Lungenschlagaderklappe liegenden VSD zu einer Kombination aus einer Lungenüberflutung, da das Blut von links nach rechts direkt über den VSD in die darüberlegende Lungenarterie geleitet wird. Gleichzeitig kommt es zu einer Zyanose im Körper, da die Hauptschlagader, die vollständig aus der rechten Kammer entspringt eher Sauerstoff-armes Blut führt. Es kommt also zu Herzinsuffizienzzeichen, also zu einer eingeschränkten Belastbarkeit und gleichzeitig zur Blaufärbung der Haut.
Ursachen und Risikofaktoren
Die Ursache für die Entstehung des DORVs, welcher etwa 3 % aller angeborenen Herzfehler ausmacht, ist noch nicht vollständig geklärt. Meist ist es das Zusammenkommen unterschiedlicher Faktoren, die zur Entwicklung dieses Herzfehlers beitragen.
Im Mutterleib kommt es bei diesem Herzfehler zu einer fehlerhaften Drehung der gemeinsamen Anlage der beiden großen Gefäße, Lungenschlagader und Aorta, welche anders als beim normalen Herzen falsch zu liegen kommen und damit größtenteils aus der rechten Herzkammer entspringen. Zusätzlich bleibt ein Loch (VSD) zwischen den beiden Kammern, welches sich in der normalen Entwicklung im Mutterleib verschließt.
Diagnose
Oft kann ein DORV schon pränatal mittels Feinultraschall diagnostiziert werden. Nach der Geburt ist oft auch eine Ultraschalluntersuchung des Herzens für die Diagnose ausreichend. Für die Operationsplanung ist zur besseren Erkennung der Lagebeziehung des VSDs und der großen Gefäße eine CT-Untersuchung und die Herstellung von Herzmodellen sehr hilfreich. Bei unklarer Anatomie der Herzkranzgefäße kann auch eine Herzkatheteruntersuchung erforderlich sein.
Eine Computertomographie (CT) kann helfen, die Operation genau planen zu können. Mit dieser Untersuchung lassen sich die Lagebeziehung des VSDs und der großen Gefäße sichtbar machen.
Therapie und Timing der Korrekturoperation
In Abhängigkeit vom Typ des DORVs haben die Patient:innen unterschiedliche Symptome, die zu unterschiedlichen Zeitpunkten auftreten können. Davon abhängig variieren der Zeitpunkt, an dem die Operation empfohlen wird sowie die Technik der Korrektur.
Gibt es keine Enge in der rechten Ausstrombahn, so sind die Symptome, die das Kind entwickelt, abhängig von der Größe des VSDs. Ist dieser groß, kommt es bereits früh zur Lungenüberflutung (DORV vom VSD-Typ). In diesem Fall muss daher ähnlich wie beim „normalen“ VSD im Alter von vier bis sechs Monaten eine Korrekturoperation erfolgen, damit sich kein irreversibler Lungenhochdruck entwickeln kann.
Besteht hingegen eine Enge der rechten Ausstrombahn, ist die Lunge zwar erstmal vor dieser Überflutung „geschützt“, allerdings kann es andererseits bei einer ausgeprägten Enge auch zu einem zu geringen Blutfluss in die Lunge und somit zur Blausucht kommen (DORV vom Fallot-Typ). Ist die Enge der rechten Ausstrombahn hochgradig ausgeprägt, kann es sein, dass es bereits früh nach der Geburt eine Zyanose gesehen wird, sodass manchmal eine palliative Operation in Form eines operativ angelegten Shunts oder eine Katheterintervention durch einen Ductusstent nötig werden, um die Lunge mit ausreichend Blut zu versorgen, bevor eine endgültige Korrektur erfolgen kann.
Liegt ein sogenannter „DORV vom TGA-Typ“, also vertauschte große Gefäße und ein VSD unterhalb der Lungenschlagaderklappe vor, kommt es kurz nach der Geburt zu ausgeprägten Herzinsuffizienzzeichen sowie zur Zyanose, weshalb eine Korrektur bereits im Neugeborenenalter angezeigt ist.
Es gibt medikamentöse sowie katheterinterventionelle Therapieoptionen, die eingesetzt werden können, um Symptome zu lindern und Zeit zu gewinnen, allerdings ist in jedem Fall eine chirurgische Korrektur des DORVs nötig. Diese sieht, je nach vorliegendem Typ des DORVs, unterschiedlich aus:
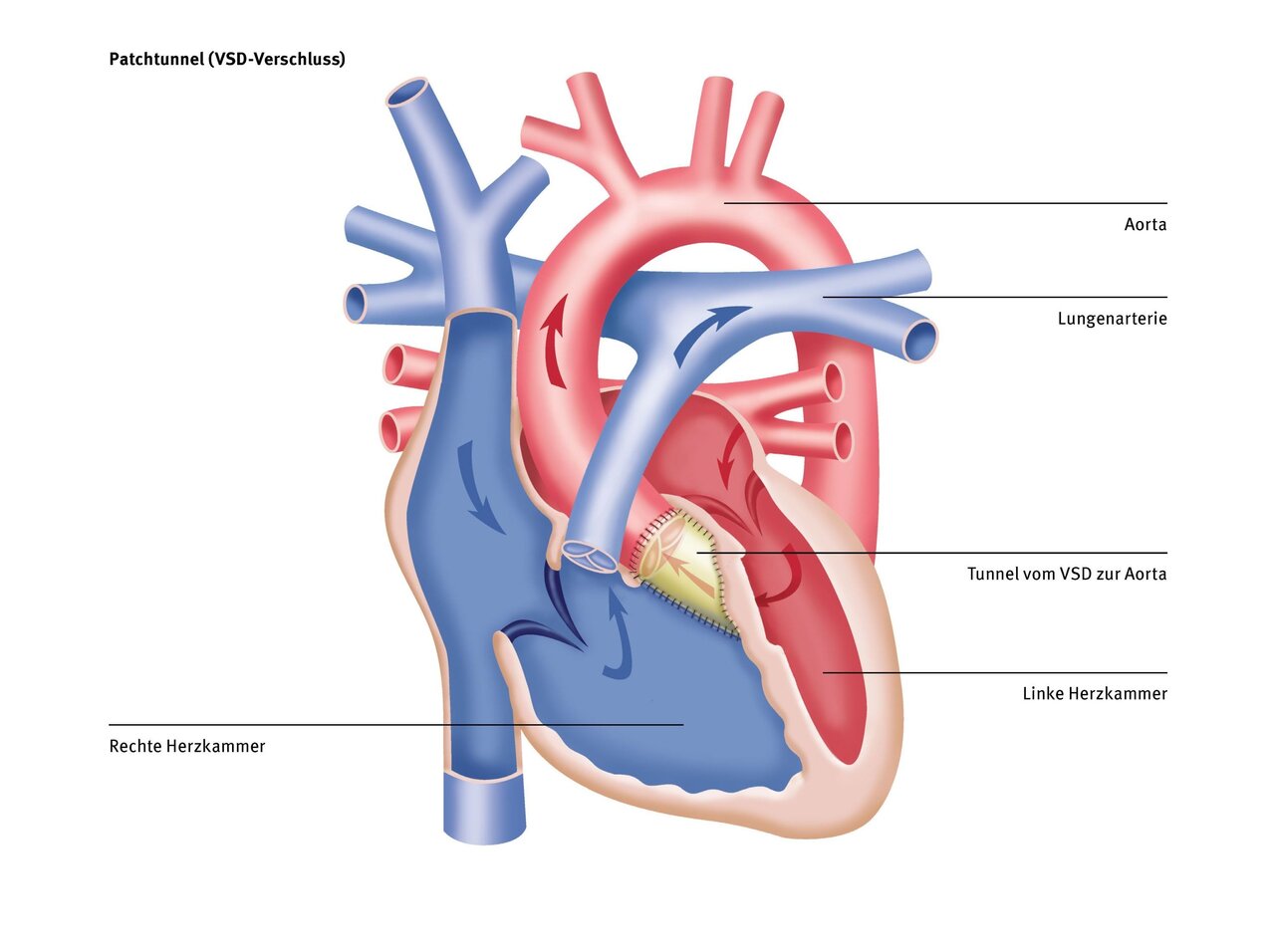
Bei diesem Typ des DORVs wird ähnlich wie beim „normalen“ VSD, ein Flicken aus eigenem Herzbeutel dazu verwendet, das Loch auf Kammerseptumebene zu verschließen und gleichzeitig eine Verbindung von der linken Herzkammer zur Aorta und von der rechten Herzkammer zur Lungenschlagader zu schaffen, die möglichst gerade und ohne Engstellen sein sollte. Um dies zu erreichen, ist es manchmal nötig, den VSD zu vergrößern, um einen möglichst geraden und engstellenfreien „Tunnel“ im Herzen zu schaffen.
Bei diesem Typ des DORVs variiert die Art des chirurgischen Eingriffs je nach Ausprägung der Engstelle im Bereich der rechten Ausstrombahn. Wenn diese so ausgeprägt ist, dass es bereits im Neugeborenenalter zur Blausucht des Kindes kommt, kann es sein, dass zunächst ein palliativer Eingriff in Form eines Shunts zwischen der Lungenarterie und der Aorta bzw. des ersten von der Aorta abgehenden Gefäßes (A. subclavia) nötig ist, um ausreichend Blut in die Lunge des Kindes zu führen, bis eine definitive Korrektur möglich ist. Diese sollte im Alter von mindestens drei bis vier Monaten bei einem Körpergewicht von weniger als 5 kg durchgeführt werden.
Die Korrektur besteht aus dem Verschluss des VSDs durch einen Flicken aus eigenem Herzbeutel. Auch hier ist es besonders wichtig, einen geraden und engstellenfreien „Tunnel“ im Herzen zu schaffen, der die linke Herzkammer mit der Aorta verbindet. Abhängig vom Schweregrad der Engstelle der rechten Ausstrombahn muss dann entweder unterhalb der Lungenschlagaderklappe das verdickte Muskelgewebe entfernt werden und/oder die Lungenschlagaderklappe repariert werden. Diese ist oft durch ein Lösen der Verwachsungen/Verklebungen der Klappentaschen oder aber durch eine Erweiterung des Klappenrings zu möglich (Kommissurotomie, Valve-Sparing-Technik, Transannulärer Patch; siehe Korrektur der Fallot’schen Tetralogie).
Ist es trotz all dieser Methoden nicht möglich die Klappe zu erhalten, beispielsweise beim Vorliegen einer Pulmonalklappenatresie, dann kommt ein sogenanntes „RV-PA-Konduit“ zum Einsatz. Dieses ist ein kleines Rohr aus Kunststoff „PTFE“ oder eine biologische Prothese, welche eine Verbindung zwischen der rechten Herzkammer und den Lungenarterien schafft.
Bei diesem Typ ist eine Korrektur bereits im Neugeborenenalter notwendig. Diese besteht aus einem „Tauschen“ der beiden großen Gefäße durch eine sogenannte „Switch-Operation“ und einer anschließenden Verbindung der linken Herzkammer zur Aorta und der rechten Herzkammer zur Lungenarterie durch den VSD-Verschluss. Auch in diesem Fall ist es besonders wichtig, einen geraden und engstellenfreien „Tunnel“ im Herzen zu schaffen, der die linke Herzkammer mit der Aorta verbindet. Wenn es beim DORV vom TGA-Typ eine Engstelle im Bereich der Pulmonalklappe (DORV-TGA + Pulmonalstenose) gibt, wird am Deutschen Herzzentrum der Charité die sogenannte `Enbloc-Rotation der Großen Gefäße´ durchgeführt. Näheres dazu finden Sie im Kapitel TGA.
Wie erwähnt ist ein gerader engstellenfreier „Tunnel“ im Herzen für eine „Zwei-Kammer Korrektur“, also eine Korrektur, die zwei getrennte Kreisläufe schafft, für die Langzeitprognose wesentlich. Ist dies trotz der Vergrößerung des VSDs u.a. durch einen den Ausflusstrakt ziehenden Klappenhalteapparat nicht möglich, so ist in manchen Fällen eine „univentrikuläre Palliation“, also die Schaffung eines „Einkammerherzens“ eine vertretbare Option (siehe „Univentrikuläre Rekonstruktion“).
Therapie am DHZC
Am Deutschen Herzzentrum der Charité haben wir uns zum Ziel gesetzt, für jede Patientin und jeden Patienten die bestmögliche chirurgische Therapieoption zu finden. Das heißt, wir analysieren im Team bestehend aus Kinderherzchirurg:innen und Kinderkardiolog:innen jede:n Patient:in und die jeweilige Herzanatomie ganz genau, um für sie bzw. ihn die beste Entscheidung treffen zu können. Wir sind dabei immer bestrebt, möglichst eine „biventrikuläre Korrektur“, also ein „Zweikammerherz“ zu schaffen, da sich dies in Studien noch immer als „physiologischer“ erwiesen hat als die „Einkammerherz“-Rekonstruktion. Dies ist leider nicht für jedes, aber für viele DORV-Herzen möglich.
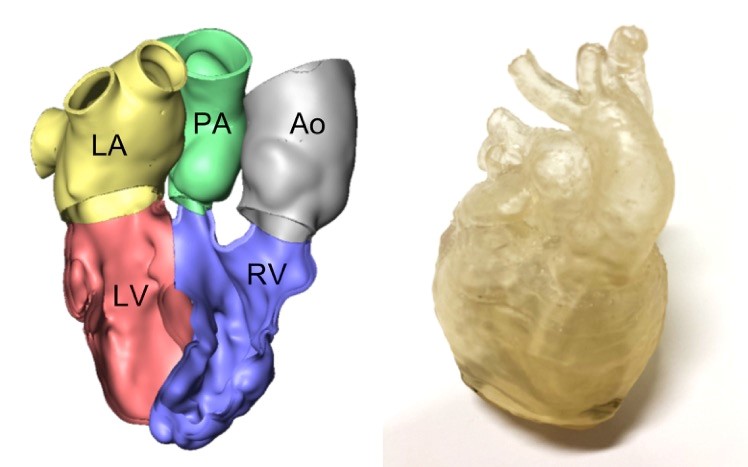
In besonders komplexen Fällen, in denen eine normale Echokardiographie nicht ausreicht, wird bei uns eine MRT- bzw. CT-Untersuchung eingesetzt. Diese Bildgebungen ermöglichen uns durch spezielle Programme einen 3D-Druck des Herzen Ihres Kindes anzufertigen, um dann eine möglich genaue Entscheidung bezüglich der optimalen chirurgischen Therapie treffen zu können. Dies hat uns schon in vielen Fällen geholfen, das Outcome der Patient:innen enorm zu verbessern.
Beispiele von 3D-rekonstruierten Herzen von DORV-Patient:innen mit komplexer Anatomie.
Auf der linken Seite: das rekonstruierte Modell am Computer.
Auf der rechten Seite: das gedruckte Modell zur besseren Darstellung.
Prognose
In Abhängigkeit von der tatsächlich durchgeführten Operation kann Ihr Kind nach unterschiedlicher Erholungszeit in den meisten Fällen wieder normal belastet werden.
Wenn zunächst ein Shunt als „Palliation“ bis zur vollständigen Korrektur angelegt werden muss, so muss in dieser Zeit die Sauerstoffsättigung im Blut genau kontrolliert werden. Es kann sein, dass das Kind in dieser Zeit auch bis zur definitiven Korrektur im Krankenhaus bleiben muss, um dort sehr genau beobachtet und betreut werden zu können.
Ist eine definitive Korrektur möglich, so gehen wir von einer normalen Belastbarkeit nach abgeschlossenem Krankenhausaufenthalt und entsprechender Erholungszeit aus. Allerdings müssen in den nächsten Wochen, Monaten und auch Jahren nach der Operation genaue Kontrollen bei der niedergelassenen Kinderkardiologin bzw. beim niedergelassenen Kinderkardiologen durchgeführt werden, um die weitere Entwicklung des Kindes genau im Blick zu behalten und eventuelle Verengungen der Ausstrombahnen sofort zu erkennen.
Das Brustbein, welches wir bei dieser Operation längs durchtrennen müssen, braucht in der Regel etwa vier bis sechs Wochen, um wieder vollständig zu verheilen und stabil zu sein. Danach steht einer normalen Belastung nichts im Wege.
Fragen und Antworten für Eltern (FAQ)
In Abhängigkeit von der tatsächlich durchgeführten Operation ist eine unterschiedliche postoperative Nachsorge notwendig. In jedem Fall sollten nach DORV-Korrektur lebenslange echokardiographische Kontrollen bei der niedergelassenen Kinderärztin bzw. beim niedergelassenen Kinderarzt erfolgen, um eventuelle Verengungen im Bereich der rechten, seltener der linken Ausstrombahn, ein zu klein gewordenes RV-PA-Konduit oder Undichtigkeiten der Aortenklappe nach einer erfolgten „Switch-Operation“ zu erkennen.
In Abhängigkeit von der tatsächlich durchgeführten Operation variieren die Lebensqualität und Lebenserwartung Ihres Kindes.
Die Lebensqualität sollte nach einer vollständigen Korrektur bis auf regelmäßige Kontrollen bei der oder dem Kinderkardiolog:in keine großen Einschränkungen haben. Kommt es im Laufe der Zeit zu Verengungen im Bereich der rechten Ausstrombahn, kann dies die Lebensqualität jedoch einschränken, weshalb ein genaues und engmaschiges Monitoring wichtig ist.
Hinsichtlich des Überlebens nach DORV-Korrektur gab es in den letzten Jahren sehr große Fortschritte. So liegt das 15-Jahres-Überleben, wenn man alle DORV-Typen zusammenfasst, bei etwa 80 %, bei einigen Typen wie dem DORV vom VSD oder Fallot-Typ sogar über 95 %.
Ob erneute Interventionen oder Operationen nötig sind, hängt sehr stark von der vorliegenden Anatomie und von der Operation ab, die aufgrund der anatomischen Verhältnisse gemacht werden konnte. Wichtig ist, dass der „Tunnel“ im Herzen, der die linke Herzkammer mit der Aorta verbindet, möglichst gerade und engstellenfrei ist. Wenn dieser eher „geschlängelt“ verläuft oder bereits zum Zeitpunkt der Operation zu Engstellen neigt, sind erneute Interventionen oder Operationen im Bereich der rechten Ausstrombahn wahrscheinlicher.
Verengungen der linken Ausstrombahn kommen hingegen seltener vor, können allerdings auftreten, wenn es im Bereich des „Tunnels“ zu Spannungen kommt. Musste die Lungenschlagaderklappe aufgrund ihrer Kleinheit durch eine sogenannte Flickenplastik erweitert werden, könnte eine erneute Operation an dieser Klappe nötig werden, da der Klappenring durch die Erweiterungsplastik nur ein begrenztes Wachstum aufweist. Insbesondere wenn ein „RV-PA“-Konduit verwendet wurde, ist ein Austausch durch ein größeres bzw. klappentragendes Konduit nötig.
Wurde eine „Switch-Operation“ beim DORV vom TGA-Typ durchgeführt, kann es an der „Neo-Aortenklappe“ zu Undichtigkeiten kommen, sodass hier eine Reoperation notwendig werden könnte. Daher sind regelmäßige echokardiographische Kontrollen bei der oder dem niedergelassenen Kinderkardiolog:in notwendig.

